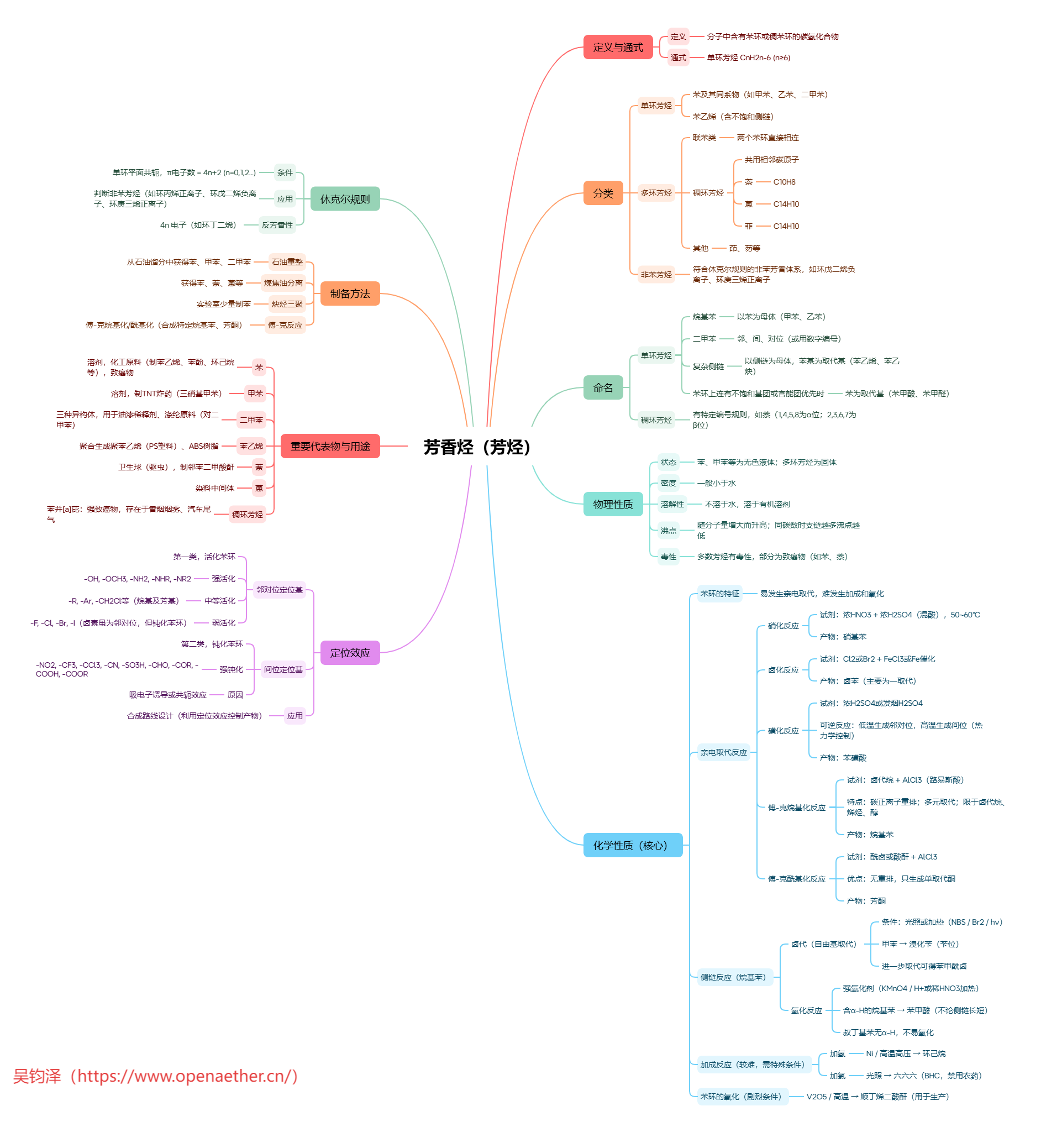
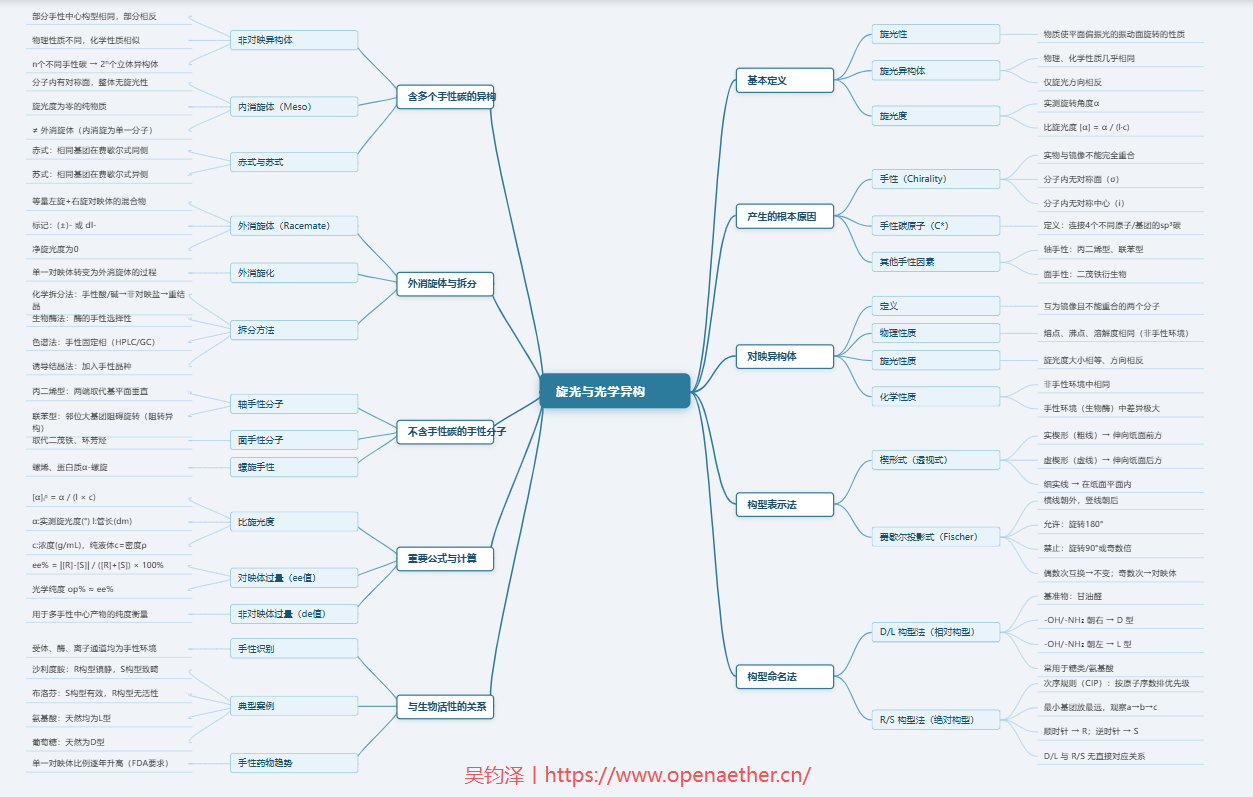
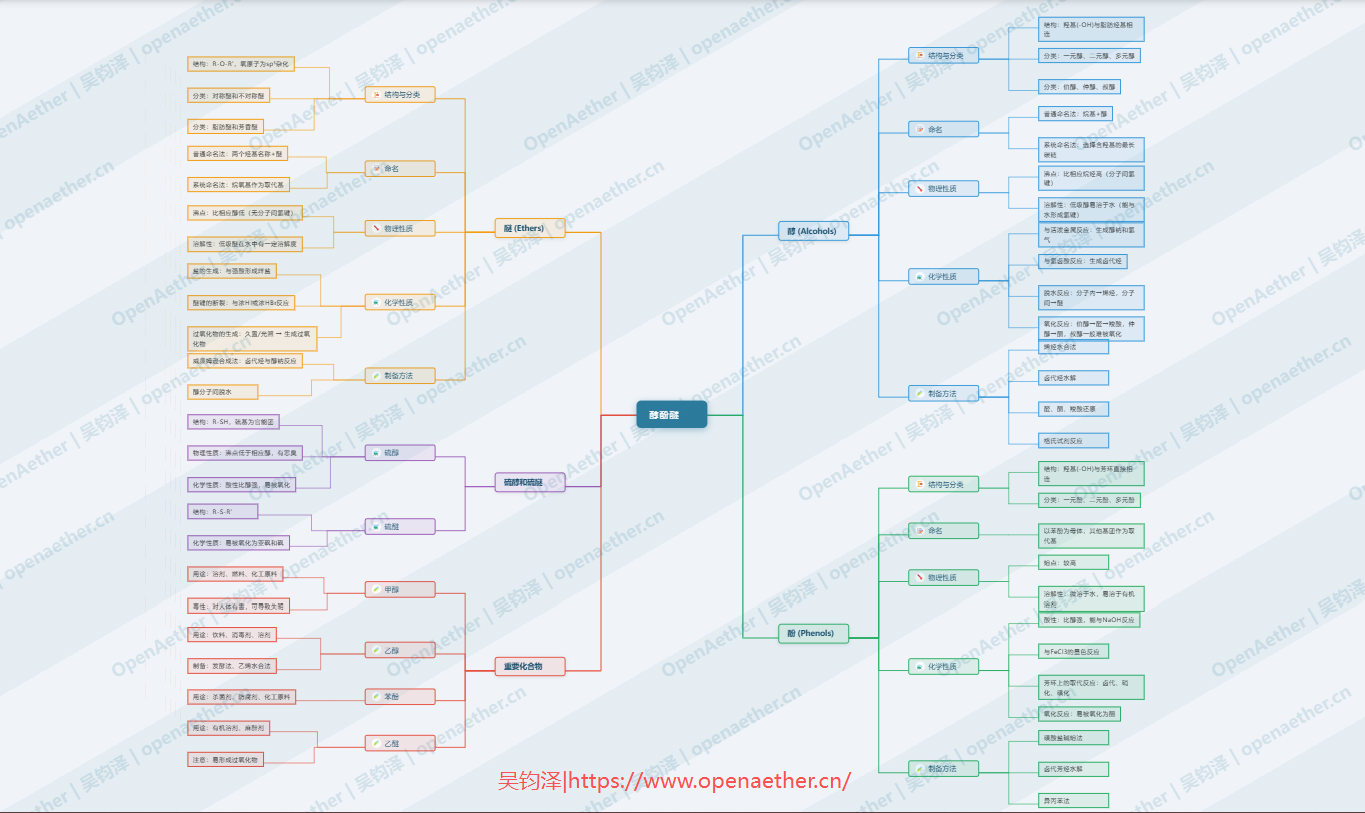
卤代烃思维导图
卤代烃
卤代烃是一类极为重要且应用广泛的化合物。它们可以看作是烃分子中的一个或多个氢原子被卤素原子(氟、氯、溴、碘)取代后生成的衍生物。正是这个看似简单的取代,赋予了卤代烃丰富多变的化学性质和广泛的实用价值。
什么是卤代烃?
卤代烃的通用结构可以表示为 R–X,其中 R 代表烷基、烯基、芳基等烃基,X 代表卤素原子(F、Cl、Br、I)。由于卤素原子的电负性远大于碳原子,C–X 键具有明显的极性,碳端带部分正电荷,这使得卤代烃成为有机合成中常用的亲电试剂和亲核取代反应底物。
根据烃基的不同,卤代烃可分为饱和卤代烃(卤代烷烃)、不饱和卤代烃(卤代烯烃、卤代炔烃)和卤代芳烃。根据卤素种类的不同,又可分为氟代烃、氯代烃、溴代烃和碘代烃。分子中若含有多个卤素原子,则称为多卤代烃。
命名规则
普通卤代烃常以烃基名称加上卤素名称来命名,如氯甲烷、溴乙烷、碘苯。系统命名法则将卤素作为取代基,编号时使卤素所在位置尽可能小,例如1-氯丙烷、2-溴丁烷。对于不饱和卤代烃,需标明双键或三键的位置,如3-氯-1-丙烯。卤代芳烃中,常见的有氯苯、苄氯(氯代甲苯)等。
物理性质
卤代烃的物理性质受卤素原子种类和数量影响显著。常温下,低分子量的卤代烃(如氯甲烷、溴乙烷)为气体或易挥发的液体,许多具有类似醚的甜味。随着碳链增长和卤素原子增多,密度和沸点升高。多数卤代烃不溶于水,但易溶于有机溶剂。值得一提的是,除氟代烃外,大多数氯、溴、碘代烃的密度大于水,这与烷烃不同。
一个有趣的规律是:同系列卤代烃中,碘代烃通常颜色较深(碘乙烷为淡黄色),且碘代烃和溴代烃在光照下易分解变色。
化学性质
卤代烃最突出的化学性质是亲核取代反应和消除反应。
亲核取代是卤代烃的标志性反应。由于卤素电负性大,C–X 键的碳原子缺电子,容易被富电子的亲核试剂(如 OH⁻、CN⁻、NH₃、RO⁻ 等)攻击,卤素以 X⁻ 形式离去。根据反应机理,亲核取代分为单分子历程(SN1)和双分子历程(SN2)。SN1 涉及碳正离子中间体,反应速率仅与卤代烃浓度有关,常见于叔卤代烃;SN2 为一步协同过程,反应速率与卤代烃和亲核试剂浓度都有关,常见于伯卤代烃。利用亲核取代可以制备醇、醚、腈、胺等多种化合物,是有机合成中的基本手段。
消除反应则是卤代烃在碱作用下脱去一分子卤化氢,生成烯烃或炔烃。消除同样有 E1 和 E2 机理。在合成中,消除反应与取代反应常常竞争,控制反应条件(温度、碱强度、溶剂极性)可以选择性地得到目标产物。
此外,卤代烃可以与金属镁反应生成格氏试剂(RMgX),这是有机化学中最重要的碳负离子等价试剂之一,广泛应用于碳链增长反应。卤代芳烃(如氯苯)的亲核取代相对困难,需要在强烈条件下才能进行,这反映了芳环的稳定性。
来源与制备
卤代烃的制备方法多种多样。实验室中常用醇与氢卤酸作用(如用浓盐酸和氯化锌与正丁醇制备氯丁烷),或通过烯烃与卤化氢、卤素的加成。工业生产则根据不同需求选择路线:甲烷的氯代可以制备氯甲烷、二氯甲烷、氯仿和四氯化碳;乙烯与氯气加成得到1,2-二氯乙烷(PVC 单体原料);苯在铁催化下氯化生成氯苯;甲苯的光氯化得到苄氯。
氟代烃的制备往往需要特殊方法,如用 SbF₃ 等氟化试剂交换氯原子。
主要用途
卤代烃在日常生活和工业生产中扮演着重要角色:
制冷剂:氯氟烃(CFCs,俗称氟利昂)曾长期用作冰箱、空调的制冷剂,但因破坏臭氧层而被逐步淘汰,现正被氢氟烃(HFCs)等替代。
溶剂:二氯甲烷(脱漆剂)、氯仿(曾用作麻醉剂,现因毒性少用)、四氯化碳(干洗剂,现因毒性及臭氧层破坏受限)、三氯乙烯(金属脱脂剂)等。
塑料原料:氯乙烯聚合为聚氯乙烯(PVC),广泛用于管材、电缆、人造革;四氟乙烯聚合为聚四氟乙烯(特氟龙),用于不粘锅涂层。
农药与医药:许多杀虫剂、除草剂、杀菌剂含有卤素原子,如滴滴涕(虽已禁用但历史上著名)、溴甲烷(土壤熏蒸剂)。医药中,氯霉素(含氯)、氟喹诺酮类(含氟)等是重要抗生素。
灭火剂:哈龙(溴氯氟烃)曾用于灭火器,但因破坏臭氧层被限制。
有机合成中间体:格氏试剂、烷基锂等从卤代烃制备,用于合成复杂分子。
本材料由华中农业大学(课程:有机化学)提供参考:
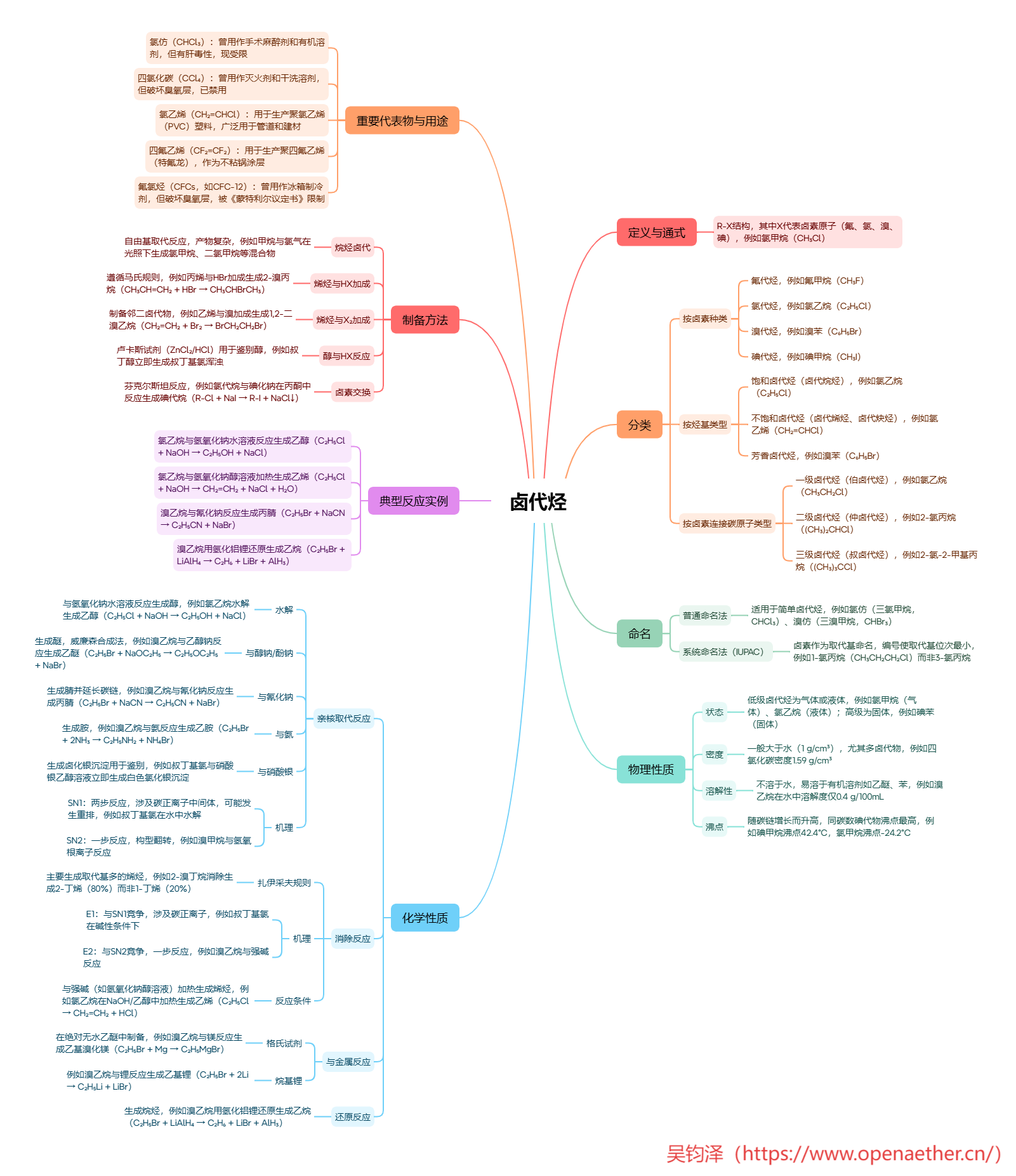
卤代烃 │ ├── 1. 定义与通式 │ └── R-X (X = F, Cl, Br, I) │ ├── 2. 分类 │ ├── 按卤素种类:氟代烃、氯代烃、溴代烃、碘代烃 │ ├── 按烃基类型: │ │ ├── 饱和卤代烃(卤代烷烃) │ │ ├── 不饱和卤代烃(卤代烯烃、卤代炔烃) │ │ └── 芳香卤代烃(如溴苯) │ └── 按卤素连接碳原子类型: │ ├── 一级卤代烃(伯卤代烃,1°) │ ├── 二级卤代烃(仲卤代烃,2°) │ └── 三级卤代烃(叔卤代烃,3°) │ ├── 3. 命名 │ ├── 普通命名法(简单卤代烃):氯仿、溴仿 │ └── 系统命名法(IUPAC):卤素作为取代基,编号使位次和最小 │ ├── 4. 物理性质 │ ├── 状态:低级为气体/液体,高级为固体 │ ├── 密度:一般 > 水(尤其是多卤代物) │ ├── 溶解性:不溶于水,溶于有机溶剂 │ └── 沸点:随碳链增长而升高,同碳数碘代物最高 │ ├── 5. 化学性质(核心) │ ├── 亲核取代反应 (SN) │ │ ├── 水解 → 醇 │ │ ├── 与醇钠/酚钠 → 醚 (威廉森合成法) │ │ ├── 与氰化钠 → 腈 (碳链增长) │ │ ├── 与氨 → 胺 │ │ ├── 与硝酸银 → 卤化银沉淀 (鉴别卤代烃) │ │ └── 机理:SN1 (两步,有重排) 与 SN2 (一步,构型翻转) │ ├── 消除反应 (E) │ │ ├── 扎伊采夫规则:主要生成取代基多的烯烃 │ │ ├── 机理:E1 (与SN1竞争) 与 E2 (与SN2竞争) │ │ └── 与强碱(如NaOH/醇)加热 → 烯烃 │ ├── 与金属反应 → 金属有机化合物 │ │ ├── 格氏试剂 (R-MgX,绝对无水乙醚中制备) │ │ └── 烷基锂 (R-Li) │ └── 还原反应 → 烷烃 (如LiAlH4 或 Zn/HCl) │ ├── 6. 典型反应实例 │ ├── 氯乙烷 → 乙醇 (NaOH/H2O) │ ├── 氯乙烷 → 乙烯 (NaOH/醇,加热) │ ├── 溴乙烷 → 乙腈 (NaCN) │ └── 溴乙烷 → 乙烷 (LiAlH4) │ ├── 7. 制备方法 │ ├── 烷烃卤代 (自由基取代,产物复杂) │ ├── 烯烃与HX加成 (马氏规则) │ ├── 烯烃与X2加成 (制备邻二卤代物) │ ├── 醇与HX反应 (卢卡斯试剂鉴别) │ └── 卤素交换 (芬克尔斯坦反应,如制碘代烃) │ └── 8. 重要代表物与用途 ├── 氯仿 (CHCl3):溶剂,曾用麻醉剂(有肝毒性) ├── 四氯化碳 (CCl4):灭火剂,溶剂(破坏臭氧层) ├── 氯乙烯:制聚氯乙烯(PVC)塑料 ├── 四氟乙烯:制聚四氟乙烯(特氟龙,不粘锅涂层) └── 氟氯烃 (CFCs):制冷剂,破坏臭氧层(已被限制)
本站所有内容除投稿内容外的均属于OpenAether网站版权所有。