乙酸异戊酯制备实验(测试)
乙酸异戊酯制备实验
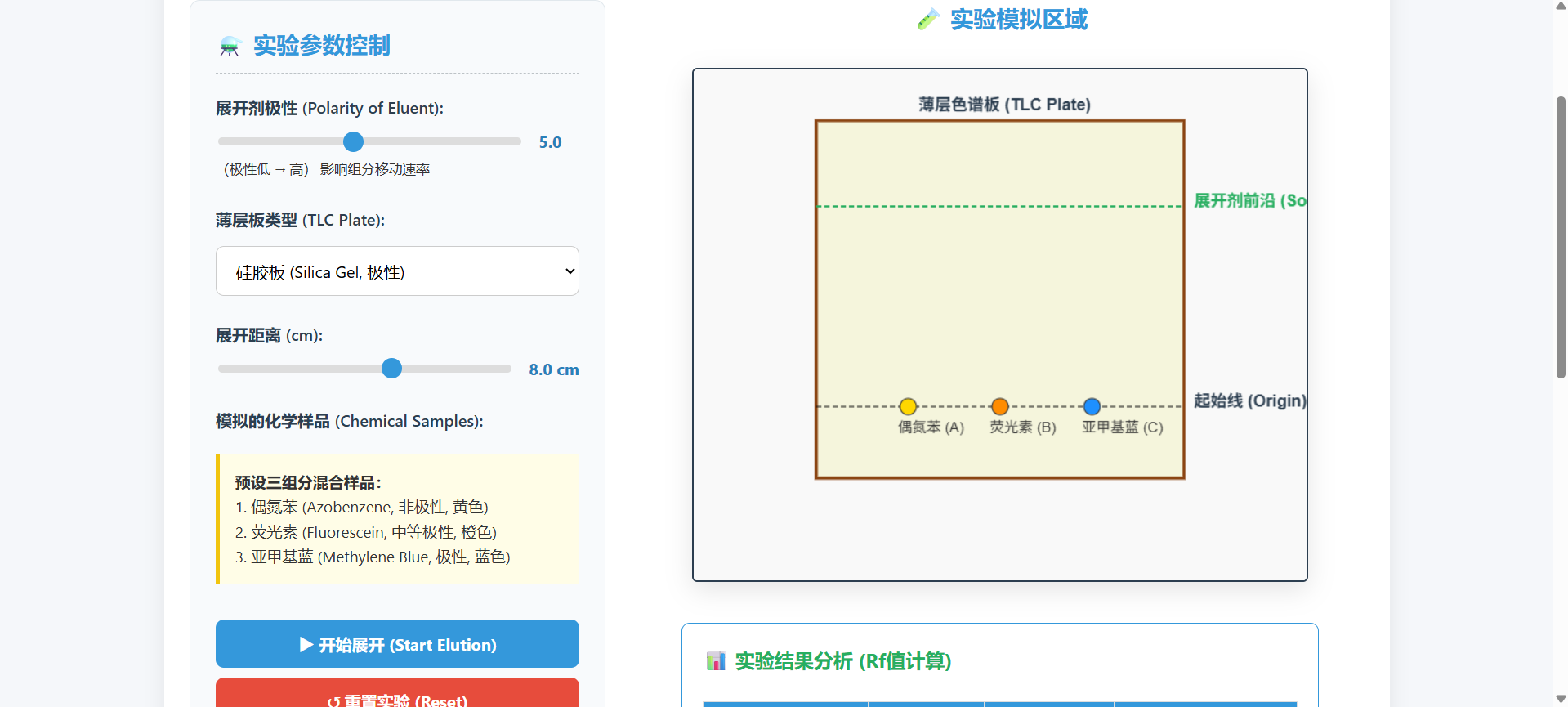
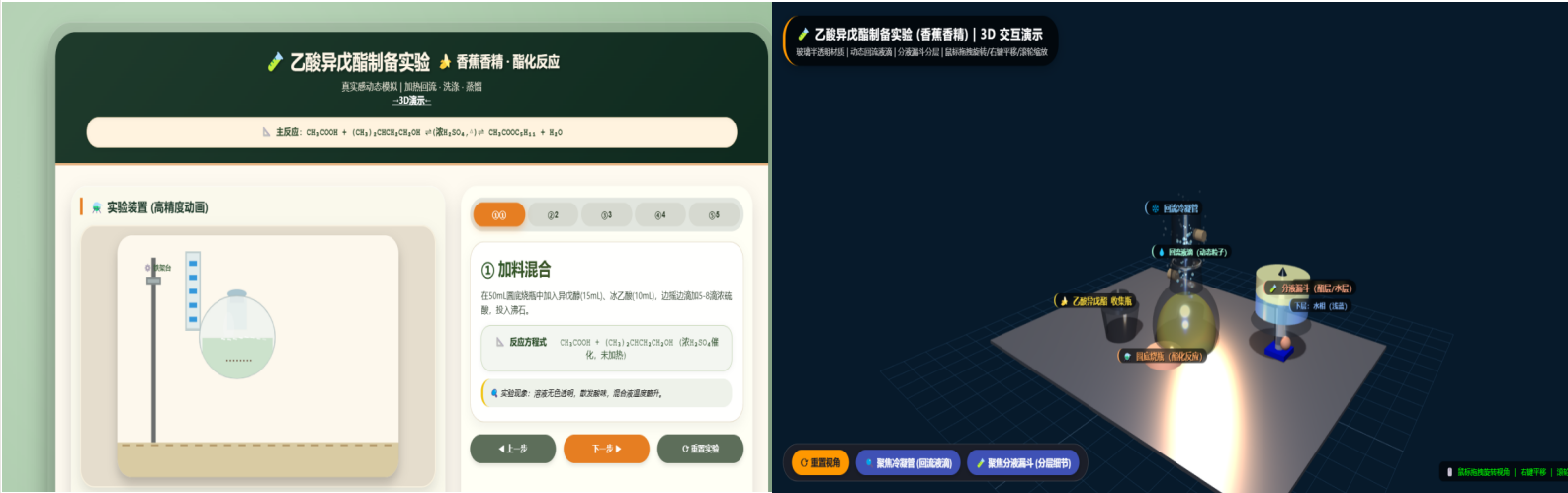 乙酸异戊酯制备实验(实验):https://www.openaether.cn/huaxue/ysywzzbsy/
乙酸异戊酯制备实验(实验):https://www.openaether.cn/huaxue/ysywzzbsy/
乙酸异戊酯制备实验(3D模拟):https://www.openaether.cn/huaxue/ysywzzbsy/3d.html
一、实验基本原理
乙酸异戊酯是由乙酸与异戊醇在酸性催化剂作用下发生酯化反应制得:
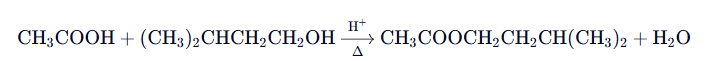
该反应为可逆反应,为提高产率需采取以下措施:
使用过量乙酸(通常乙酸:异戊醇=2.25:1),使平衡向生成酯的方向移动。
通过分水器及时移除生成的水,降低产物浓度,促使反应正向进行。
加入带水剂(如环己烷),与水形成共沸物,便于水的分离。
二、实验装置与仪器
1. 核心装置
带分水器的回流装置:包括圆底烧瓶(反应容器)、球形冷凝管、分水器。
蒸馏装置:用于产物的精制纯化。
2. 关键仪器
圆底烧瓶(100mL)。
分水器(Dean-Stark Trap型)。
球形冷凝管(冷却水从b口进,a口出,下进上出)。
分液漏斗(100mL)。
无水硫酸镁(干燥剂)。
三、实验步骤详解
1. 酯化反应
加料:在干燥圆底烧瓶中加入18mL异戊醇、24mL冰醋酸,在振摇下缓慢加入2.5mL浓硫酸,再加几粒沸石。
安装装置:连接带分水器的回流装置,分水器中预先充水至支管口略低处,并放出比理论出水量稍多的水。
加热回流:用甘油浴或电热套加热,保持回流状态,反应时间约1.5小时,至分水器中水层不再增加。
2. 洗涤纯化
水洗:反应液冷却后倒入分液漏斗,用30mL冷水淋洗烧瓶内壁,洗涤液并入分液漏斗。
碱洗:用20mL 10%碳酸氢钠溶液分两次洗涤,除去未反应的乙酸。
盐洗:最后用10mL饱和氯化钠溶液洗涤一次,降低酯在水中的溶解度。
3. 干燥与蒸馏
干燥:有机层由分液漏斗上口倒入干燥锥形瓶,加入约2g无水硫酸镁,振摇至液体澄清,静置20-30分钟。
蒸馏:将干燥好的粗酯滤入蒸馏烧瓶,蒸馏收集138-142℃馏分,称量质量并计算产率。
四、关键操作要点
1. 分水器使用技巧
分水器中水量不再增加时,表明反应基本完成,可停止加热。
实验过程中需持续关注分水器中液面变化,适时放出部分水,确保有机相能顺利回流。
分水器工作原理:利用有机物与水不互溶且密度比水小的特性,使有机相在上层流回反应瓶,水留在分水器中。
2. 产率提高策略
增加乙酸用量可提高异戊醇的转化率,但过量乙酸会导致体系温度降低,反而降低产率。
催化剂选择:传统使用浓硫酸,但NH₄Fe(SO₄)₂·12H₂O等新型催化剂可提高产率至89.63%,且更环保。
带水剂优化:环己烷用量为10mL时效果最佳,过多会降低回流温度。
3. 产率计算
理论产量:根据异戊醇的物质的量计算(异戊醇为限制性反应物)。
实际产率:


典型产率:传统方法约75%,优化后可达86.3%。
五、实验教学价值
1. 知识目标
深入理解酯化反应的可逆性及化学平衡移动原理。
掌握分水回流装置在可逆反应中的应用必要性。
2. 能力目标
培养反应装置设计选择能力,理解分水器的创新设计思维。
学会根据反应物性质优选分析方法(如酸值法、气相色谱法)。
掌握液态有机物的分离纯化技术(萃取、干燥、蒸馏)。
3. 素质目标
培养团结协作精神,通过小组讨论完成实验设计。
增强环保意识,对比不同催化剂的环境影响。
培养严谨的科学态度和实验操作规范性。
六、常见问题与解决方案
产率偏低原因:
加热过快导致产品炭化。
浓硫酸催化产生副反应。
振荡混合不充分。
回流速度过快。
分水器使用技巧:
若有机相无法顺利回流,可适当放出部分水。
当观察到水层高度不再变化时,反应已达平衡。
催化剂选择:
传统浓硫酸:产率约75%,但腐蚀性强、污染大。
NH₄Fe(SO₄)₂·12H₂O:产率约89.63%,可回收利用,更环保。
磺化硅胶固体酸:可重复使用,符合绿色化学理念。
本站所有内容除投稿内容外的均属于OpenAether网站版权所有。